Описание
Выражение для константы равновесия имеет вид: 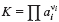 , где
, где ![]() — коэффициент в уравнении реакции для соответствующего вещества (положительный для продуктов и отрицательный для реагентов), а
— коэффициент в уравнении реакции для соответствующего вещества (положительный для продуктов и отрицательный для реагентов), а ![]() — активность данного вещества, т. е. величина, характеризующая работу перенесения малой его доли в рассматриваемую реакционную систему из некоторого стандартного состояния.
— активность данного вещества, т. е. величина, характеризующая работу перенесения малой его доли в рассматриваемую реакционную систему из некоторого стандартного состояния.
Например, для веществ, образующих несмешивающиеся чистые фазы, активность равна единице; в сильно разбавленных растворах за активность принимают концентрацию, для разреженных газов — парциальное давление и т. д. В состоянии равновесия рассчитанная по вышеприведенной формуле ![]() должна быть постоянной величиной, сохраняющейся (с учетом изменения активностей) при добавлении любых компонентов и зависящей только от температуры, а также (кроме некоторых модельных случаев) давления. Если
должна быть постоянной величиной, сохраняющейся (с учетом изменения активностей) при добавлении любых компонентов и зависящей только от температуры, а также (кроме некоторых модельных случаев) давления. Если ![]() , равновесие смещено в сторону продуктов; если
, равновесие смещено в сторону продуктов; если ![]() — в сторону реагентов.
— в сторону реагентов.
Авторы
- Еремин Вадим Владимирович
- Смирнов Андрей Валентинович
Источник
- IUPAC. Compendium of Chemical Terminology. 2nd ed. (the «Gold Book») / Compiled by A.D. McNaught, A. Wilkinson. — Oxford: Blackwell Scientific Publications, 1997. XML on-line corrected version: goldbook.iupac.org, 2006. Created by M. Nic, J. Jirat, B. Kosata. Updates compiled by A. Jenkins. Last update 07.09.2009.
