Описание
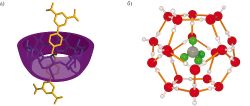
Клатраты подразделяют на два больших класса в зависимости от свойств соединения-хозяина. Молекулярные клатраты образуются «хозяевами», имеющими внутримолекулярные полости (рис. а); такие клатраты могут существовать как в растворе, так и в кристаллическом состоянии. Если «хозяин» способен образовывать только межмолекулярные или кристаллические полости, то из него получаются решетчатые клатраты (рис. б) — они устойчивы лишь в твердом состоянии.
В любых клатратах между «хозяевами» и «гостями» образуются слабые межмолекулярные связи — ван-дер-ваальсовы или водородные. Клатраты — нестехиометрические соединения, в которых соотношение между числом молекул «гостя» и «хозяина» не обязательно целое, например, Cl2·5,75H2O.
Важный пример решетчатого клатрата — гидрат метана, в котором молекулы метана заключены в пустоты кристаллической решетки льда. Это соединение широко распространено в природе; запасы метана на дне океанов, вероятно, значительно превышают запасы газа в свободном состоянии.
Образование клатратов используется в хроматографии, для хранения газов и высокотоксичных веществ, опреснения морской воды и разделения соединений, близких по свойствам, но отличающихся геометрией молекул, например, цистранс-углеводородов. В последнее время активно исследуется возможность применения клатратов на основе воды и металлоорганических каркасов для аккумулирования и хранения водорода.
Иллюстрации
|
а — Соединение циклодекстрин–ротаксан — пример молекулярного клатрата. б — Гидрат метана — пример решетчатого клатрата. |
Автор
- Еремин Вадим Владимирович
Источники
- Стид Дж. В., Этвуд Дж.Л. Супрамолекулярная химия. Т. 1. — М.: Академкнига, 2007. — 479 с.
- Клатраты // Химическая энциклопедия. Т. 2. — М.: Большая Российская энциклопедия, 1990. С. 403–404.
- Манаков А.Ю., Скиба С.С. Использование клатратных соединений для хранения водорода // Российский химический журнал. 2006. Т. 50, №6. С. 73–82.
